Електрон в атомі знаходиться у постійному русі навколо ядра. Для опису стану електрона оцінюється ймовірність його знаходження у навколоядерній області простору і використовуються поняття «електронна хмара», «електронна орбіталь».
Електрони розміщені навколо ядра на енергетичних рівнях. Кожен рівень складається з підрівнів. На кожному підрівні є певна кількість орбіталей: на s-підрівні одна, на р-підрівні три, на d-підрівні пять і на f- сім.
Ядро оточене електронами. Кількість електронів дорівнює кількості протонів у ядрі, кількість протонів визначає порядковий номер елемента в періодичній системі. У нейтральному атомі сумарний негативний заряд електронів дорівнює позитивному зарядові протонів.
Спільна електронна хмара атома утворюється електронними хмарами окремих електронів. Ту частину електронної хмари електрона, у якій він перебуває більшу частину часу, називають атомною орбіталлю. Отже, атомна орбіталь – це частина простору навколо ядра, де перебування електрону найімовірніше.
Ηλεκτρόνιο) — стабільна, негативно заряджена елементарна частинка, що входить до складу всіх атомів. Має електричний заряд (−e = −1,6021892(46)×10−19 Кл) і масу (9,109554(906)×10−31 кг). Зазвичай електрон позначається в формулах символом e-.
Підрівні оболонок
| Позначення | Орбітальне квантове число | Максимальна кількість електронів |
|---|---|---|
| f | 3 | 14 |
| g | 4 | 18 |
| h | 5 | 22 |
| i | 6 | 26 |
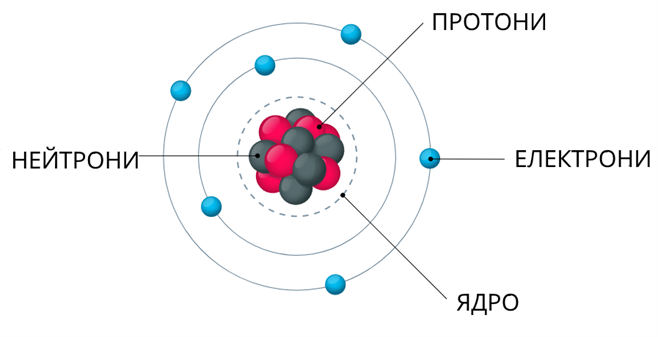
Електрони в атомі Розгляньмо, яке місце займають електрони в атомі. Якщо ядро становить 99,86 % від маси, а, як відомо, що кількість протонів і електронів дорівнює.