Радіуси атомів елементів у періоді зменшуються зліва направо. Зліва направо зростає заряд ядра і кількість електронів на зовнішньому рівні. Електрони сильніше притягуються до ядра, радіус атома зменшується.30 жовт. 2022 р.
Радіуси атомів в кожному періоді зменшуються зліва на право, а в групі збільшуються зверху до низу. Хімічні властивості атомів обумовлені їх здатністю віддавати електрони або їх приймати.
В періодах орбітальні атомні радіуси відповідно до збільшення заряду ядра Z монотонно зменшуються через зростання сили взаємодії зовнішніх електронів з ядром. В групах радіуси в основному збільшуються через збільшення кількості електронних оболонок.
Періодичність властивостей елементів Атомний радіус — збільшується зверху до низу і зменшується зліва направо (в елементах головних груп) Електронегативність — зменшується зверху до низу і збільшується зліва направо (виняток Інертні гази)
Радіус атома визначається числом енергетичних рівнів в ньому. Чим більше рівнів заповнено електронами, тим більше радіус атома.
Неметалічні властивості в періодах посилюються зліва направо. У кожному періоді найбільш виражені неметалічні властивості у елементів VIIA групи (у галогенів). У періодах неметалічні властивості посилюються, а в групах — слабшають.
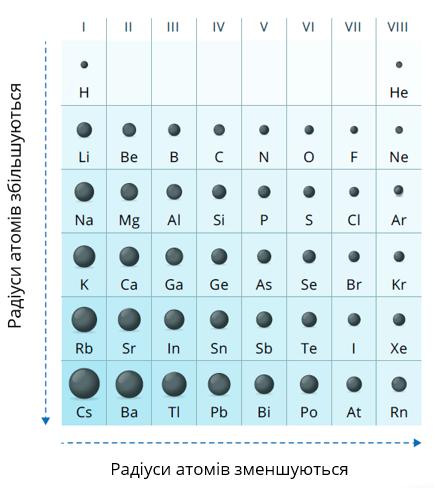

Зміна радіусів атомів в періодах В елементах одного періоду число енергетичних рівнів в атомах є однаковим. Збільшуються заряд ядра і число зовнішніх електронів .