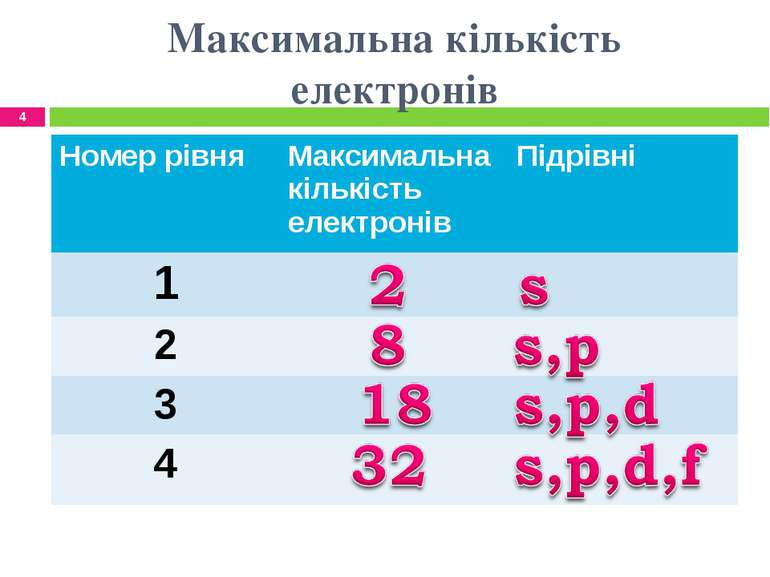
Встановлено, що максимальне число електронів на енергетичному рівні дорівнює 2n², де n — його номер. Отже, на першому рівні може перебувати не більше 2 електронів, на другому — не більше 8, на третьому — не більше 18, тощо.
– р-підрівень містить три р-орбіталі ( ), тому на ньому може перебувати максимально шість р-електронів; – d-підрівень налічує п'ять орбіталей ( ), максимальне число d-електронів – 10; – f-підрівень налічує сім орбіталей ( ), для їх заповнення знадобиться чотирнадцять f-електронів.
Число орбіталей на енергетичних рівнях різне, воно дорівнює n2, де n — номер рівня. На першому рівні (n = 1) одна 8-орбіталь, на другому (n = 2) — чотири: одна s- і три р-орбіталі, на третьому (n = 3) — дев'ять: одна три р- і п'ять d-орбіталей (див.
Максимальна кількість електронів на кожному рівні обчислюється за формулою: N = 2n2. Число енергетичних рівнів дорівнює номеру періоду, в якому перебуває хімічний елемент. Отже, електронна оболонка атомів елементів першого періоду містить один енергетичний рівень, другого періоду – два, третього – три і т. д.
Кількість електронів в кожній оболонці
| рівень/підрівень | 0 (s) | Всього в оболонці |
|---|---|---|
| 4 (N) | 2 | 32 |
| 5 (O) | 2 | 50 |
| 6 (P) | 2 | 72 |
| 7 (Q) | 2 | 98 |
Максимальна кількість електронів на одному s-підрівні — 2. Максимальна кількість електронів на одному p-підрівні — 6.

Максимальна кількість електронів 3 енергетичному рівні. Ответ. 8 людям это помогло. profile. Pantera50505. report flag outlined. Відповідь: 18. Пояснення: У 1 енергетичному рівні – 2 електрона. У 2 рівні – 8. У 3 рівні – 8. …